



版權說明:本文檔由用戶提供并上傳,收益歸屬內容提供方,若內容存在侵權,請進行舉報或認領
文檔簡介
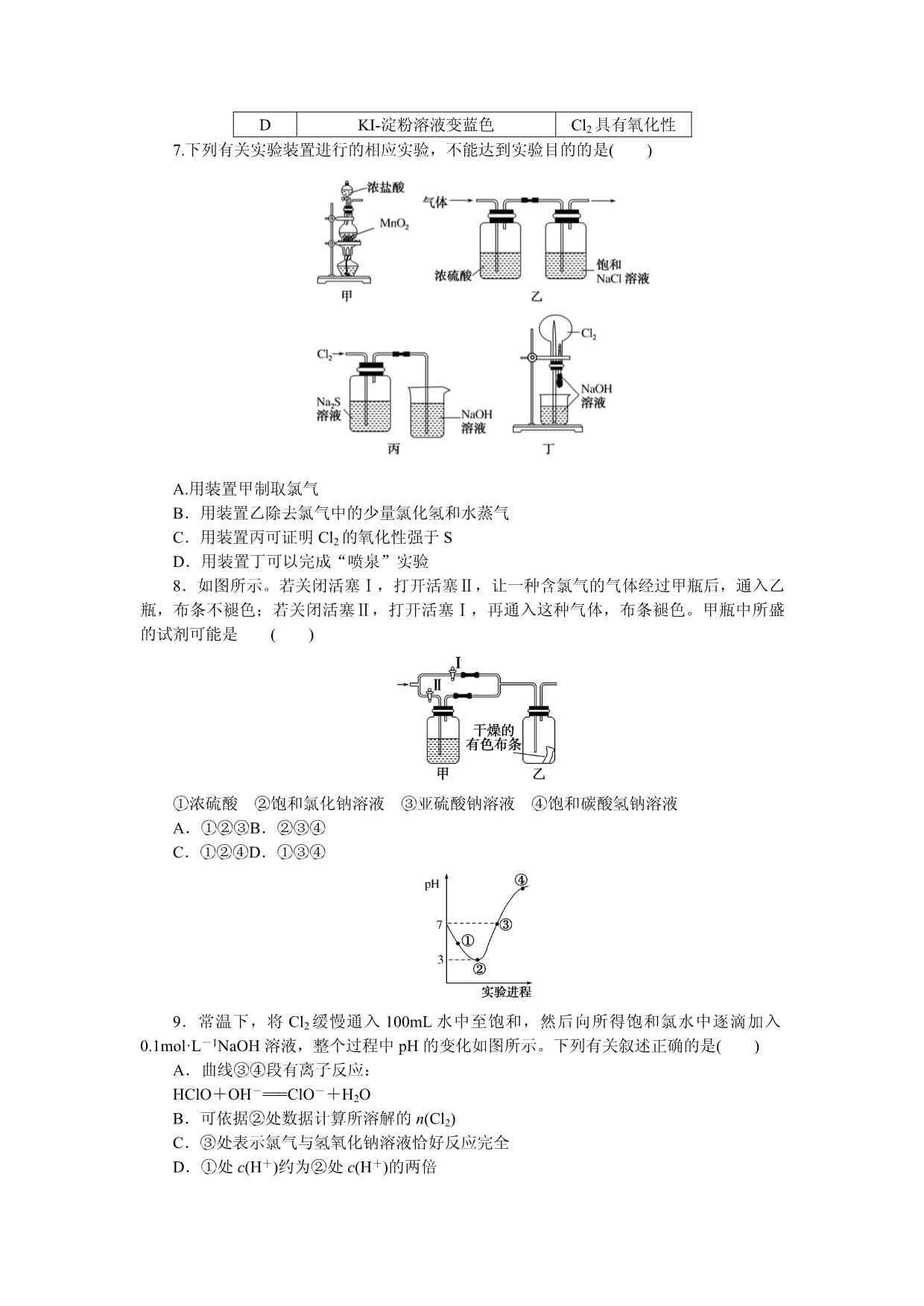
課時作業11氯及其化合物鹵素一、選擇題1.化學來源于生活,也服務于生活。下列有關生活中的化學知識敘述正確的是()A.氯氣和活性炭均可作為漂白劑,若同時使用,漂白效果會明顯加強B.氯氣與燒堿溶液或石灰乳反應都能得到含氯消毒劑C.測定溶液pH的實驗中,用干燥pH試紙測定新制氯水的pH——測定結果無影響D.潔廁靈不能與“84”消毒液混用,原因是兩種溶液混合產生的HClO易分解2.鹵族元素及其化合物在生活中應用廣泛。下列有關說法正確的是()A.氟氯烴作制冷劑會加劇霧霾天氣的形成B.只通過電解的方法就能實現從食鹽水到“84”消毒液的生產C.加碘食鹽中含有碘元素,能使淀粉溶液變藍D.工業上制漂白粉,所得的氯化物都具有漂白性3.向下列溶液中通入氯氣,現象和結論描述正確的是()A.品紅溶液:紅色褪去,加熱該褪色溶液,仍無色;氯氣具有漂白性B.紫色石蕊溶液:先變紅,后褪色;氯氣與水反應生成鹽酸和次氯酸C.含酚酞的氫氧化鈉溶液:紅色褪去;氯氣只作氧化劑D.硫化鈉溶液:溶液變渾濁;氯氣只作還原劑4.下列敘述中正確的是()A.液溴易揮發,在存放液溴的試劑瓶中應加水封B.能使潤濕的淀粉-KI試紙變成藍色的物質一定是Cl2C.某溶液加入CCl4,CCl4層顯紫色,證明原溶液中存在I-D.某溶液加入BaCl2溶液,產生不溶于稀硝酸的白色沉淀,該溶液一定含有Ag+5.下列實驗過程中,沒有發生氧化還原反應的是()6.已知:KClO3+6HCl(濃)=KCl+3Cl2↑+3H2O,如圖所示,將少量試劑分別放入培養皿中的相應位置,實驗時將濃鹽酸滴在KClO3晶體上,并用表面皿蓋好。下表中由實驗現象得出的結論完全正確的是()選項實驗現象結論A滴有KSCN的FeCl2溶液變紅色Cl2具有還原性B滴有酚酞的NaOH溶液褪色Cl2具有酸性C紫色石蕊溶液先變為紅色后褪色Cl2具有漂白性DKI-淀粉溶液變藍色Cl2具有氧化性7.下列有關實驗裝置進行的相應實驗,不能達到實驗目的的是()A.用裝置甲制取氯氣B.用裝置乙除去氯氣中的少量氯化氫和水蒸氣C.用裝置丙可證明Cl2的氧化性強于SD.用裝置丁可以完成“噴泉”實驗8.如圖所示。若關閉活塞Ⅰ,打開活塞Ⅱ,讓一種含氯氣的氣體經過甲瓶后,通入乙瓶,布條不褪色;若關閉活塞Ⅱ,打開活塞Ⅰ,再通入這種氣體,布條褪色。甲瓶中所盛的試劑可能是()①濃硫酸②飽和氯化鈉溶液③亞硫酸鈉溶液④飽和碳酸氫鈉溶液A.①②③B.②③④C.①②④D.①③④9.常溫下,將Cl2緩慢通入100mL水中至飽和,然后向所得飽和氯水中逐滴加入0.1mol·L-1NaOH溶液,整個過程中pH的變化如圖所示。下列有關敘述正確的是()A.曲線③④段有離子反應:HClO+OH-=ClO-+H2OB.可依據②處數據計算所溶解的n(Cl2)C.③處表示氯氣與氫氧化鈉溶液恰好反應完全D.①處c(H+)約為②處c(H+)的兩倍10.二氧化氯(ClO2)是一種黃綠色易溶于水的氣體,常用于飲用水消毒。下列有關ClO2的制備與殺菌的說法不合理的是()A.NaClO2在酸性條件下歧化生成ClO2和NaCl,則n(氧化劑)∶n(還原劑)=1∶4B.ClO2在強堿性環境中使用失效,可能的原因是2ClO2+2OH-=ClOeq\o\al(\s\up1(-),\s\do1(3))+ClOeq\o\al(\s\up1(-),\s\do1(2))+H2OC.可用飽和食鹽水除去ClO2中的NH3D.等物質的量的ClO2殺菌效果比Cl2強二、非選擇題11.實驗室制備氯酸鉀、次氯酸鈉和氯水的裝置如下圖所示。(1)制備KClO3需在70~80℃進行,寫出制備KClO3的離子方程式:________________________________________________________________________________________________________________________________________________。若有少量MnO2進入裝置B,則會生成K2MnO4,此反應的化學方程式是________________________________________________________________________________________________________________________________________________。(2)制備NaClO需在0~5℃進行,實驗中宜采取的措施是____________。溫度過高還會生成NaClO3,當n(NaClO)∶n(NaClO3)=1∶a時,該反應中n(Cl2)∶n(NaOH)=________。(3)制取氯酸鹽和次氯酸鹽條件的差異是________。(4)KClO3、KCl的溶解度曲線如下圖所示。反應結束后,從裝置B中獲得氯酸鉀晶體的實驗方法是________________________________________________________________________。12.某學生設計如下實驗裝置利用氯氣與潮濕的消石灰反應制取少量漂白粉(這是一個放熱反應),據此回答下列問題:(1)A儀器的名稱是____________,D的作用是________________________________________________________________________。(2)漂白粉將在U形管中產生,其反應的化學方程式是________________________________________________________________________。(3)有同學建議在兩個橡膠套管內的玻璃管口應盡量緊靠,原因是________________________________________________________________________。(4)此實驗結果所得Ca(ClO)2產率太低。經分析并查閱資料發現主要原因是在U形管中存在副反應:溫度較高時氯氣與消石灰反應生成了Ca(ClO3)2,為避免此副反應的發生,可采取的措施是____________________,有同學測出了反應后溶液中ClO-、ClOeq\o\al(\s\up1(-),\s\do1(3))兩種離子的物質的量(n)與反應時間(t)的關系曲線,粗略表示為如圖2(不考慮氯氣和水的反應)。圖2中曲線Ⅰ表示________的物質的量隨反應時間變化的關系。課時作業11氯及其化合物鹵素1.解析:A項,活性炭具有吸附性,可以吸附氯氣,錯誤;B項,氯氣與燒堿溶液或石灰乳反應均可生成次氯酸鹽,正確;C項,氯水中的次氯酸具有漂白性,錯誤;D項,不能混用的原因是消毒液中的NaClO與潔廁靈中的HCl反應生成Cl2,錯誤。答案:B2.解析:氟氯烴作制冷劑會加劇臭氧層空洞的形成,A項錯誤;電解氯化鈉溶液時生成的Cl2和NaOH會發生反應,生成含NaClO的“84”消毒液,B項正確;加碘食鹽中碘元素不是以單質形式存在的,不能使淀粉溶液變藍,C項錯誤;漂白粉中的氯化鈣沒有漂白性,D項錯誤。答案:B3.解析:A項,氯氣與水反應生成的次氯酸具有漂白性,能使品紅溶液褪色,且加熱已褪色的溶液,溶液不會恢復原來的顏色,錯誤;B項,氯氣與水反應生成鹽酸和次氯酸,鹽酸使紫色石蕊溶液變紅,次氯酸具有漂白性,能使變紅的石蕊溶液褪色,正確;C項,氯氣和NaOH溶液反應生成氯化鈉、次氯酸鈉和水,其中,氯氣既作氧化劑,又作還原劑,次氯酸鈉的漂白性和溶液堿性的減弱均會使溶液的紅色褪去,錯誤;D項,Cl2+Na2S=2NaCl+S↓,溶液變渾濁,氯氣作氧化劑,錯誤。答案:B4.解析:溴易揮發,密度比水大,實驗室常用水封的方法保存,故A正確;能使潤濕的淀粉—KI試紙變藍的物質具有氧化性,可能為NO2、O3、Cl2等物質,故B錯誤;CCl4層顯紫色證明原溶液中存在I2,故C錯誤;加入BaCl2溶液產生不溶于稀HNO3的白色沉淀,可能是AgCl或BaSO4,不一定含Ag+,故D錯誤。答案:A5.解析:A項,氯水中的HClO見光會分解生成氧氣;C項,氯水滴入NaBr溶液中,反應生成Br2和NaCl;D項,H2O與Na2O2反應產生O2,A、C、D三項都是氧化還原反應;B項,久置氯水中是HCl與發酵粉中的NaHCO3反應生成CO2,是非氧化還原反應。答案:B6.解析:A項是因為Cl2具有強氧化性,A項錯;Cl2本身沒有酸性,溶液褪色,可能是Cl2與水反應生成HCl和HClO,再與NaOH溶液發生中和反應生成鹽而使溶液褪色,還可能是生成的HClO的漂白性使溶液褪色,B項錯;Cl2本身不具有漂白性,而是Cl2與H2O作用生成的HClO具有漂白性,C項錯。答案:D7.解析:實驗室用二氧化錳與濃鹽酸在加熱的條件下反應制取氯氣,故A正確;應將氣體先通入飽和食鹽水中除去HCl氣體,再通入濃硫酸除去水蒸氣,故B錯誤;由Cl2+Na2S=2NaCl+S↓可知,Cl2可以置換出S,說明Cl2的氧化性強于S,故C正確;Cl2能被NaOH溶液吸收,使燒瓶內外產生壓強差,從而引發噴泉現象,故D正確。答案:B8.解析:Cl2與H2O反應生成的HClO具有漂白作用。氣體通過甲瓶后不能使有色布條褪色,可能有兩個原因:一是甲瓶中溶液將Cl2干燥,二是甲瓶中溶液能吸收Cl2。濃H2SO4具有吸水性,Na2SO3溶液、飽和NaHCO3溶液都能與Cl2發生反應。答案:D9.解析:曲線從②到③,溶液pH增大,說明此段發生反應:HCl+NaOH=NaCl+H2O、HClO+NaOH=NaClO+H2O,離子反應分別為H++OH-=H2O、HClO+OH-=H2O+ClO-,③點此時c(H+)=c(OH-),c(Na+)=c(Cl-)+c(ClO-),溶液中存在HClO,從③到④圖像分析可知:溶液pH繼續增大,且pH大于7,繼續加氫氧化鈉,氫氧化鈉和次氯酸反應:HClO+NaOH=NaClO+H2O,曲線③④段有離子反應:HClO+OH-=H2O+ClO-,故A正確;②點所示溶液中發生反應:Cl2+H2O?H++Cl-+HClO,HClO為弱電解質,部分電離,無法根據pH計算參加反應的氯氣,故B錯誤;氯氣與氫氧化鈉恰好反應完全為氯化鈉、次氯酸鈉溶液,溶液呈堿性,故C錯誤;①處到②處是氯氣的溶解平衡:Cl2+H2O?H++Cl-+HClO向右進行的過程,酸性逐漸增強,氫離子濃度逐漸增大,故D錯誤。答案:A10.解析:A項,酸性條件下ClOeq\o\al(\s\up1(-),\s\do1(2))發生歧化反應,生成Cl-和ClO2,可寫出方程式:4H++5ClOeq\o\al(\s\up1(-),\s\do1(2))=Cl-+4ClO2↑+2H2O,顯然氧化劑與還原劑的物質的量之比為1∶4,正確;B項,方程式符合歧化反應化合價的變化,正確;C項,ClO2易溶于水,不能用飽和食鹽水除雜,錯誤;D項,等物質的量的ClO2作氧化劑時得電子數比Cl2得電子數多,正確。答案:C11.解析:(2)當n(NaClO)∶n(NaClO3)=1∶a時,依據得失電子守恒,(3a+1)Cl2+(6a+2)NaOH=aNaClO3+NaClO+(5a+1)NaCl+(3a+1)H2O,該反應中n(Cl2)∶n(NaOH)=1∶2。(4)由溶解度曲線分析可知,同一溫度下KCl溶解度比KClO3大,溫度越高溶解度越接近,故從裝置B中獲得氯酸鉀晶體的實驗方案是冷卻結晶、過濾、洗滌。答案:(1)3Cl2+6OH-eq\o(=,\s\up7(70℃~80℃))5Cl-+ClOeq\o\al(\s\up1(-),\s\do1(3))+3H2O3MnO2+KClO3+6KOH=3K2MnO4+KCl+3H2O(或Cl2+4KOH+MnO2=K2MnO4+2KCl+2H2O)(2)將裝置C放在冰水浴中1∶2(3)堿溶液(或反應物)的濃度不同,反應溫度不同(4)將裝置B中的試管放在冰水中冷卻,過濾,用少量冰水洗滌晶體2~3次。12.解析:(1)裝置中添加濃鹽酸用的是分液漏斗;NaOH溶液的作用是吸收過量的氯氣。(2)漂白粉將在U形管中產生,反應的化學方程式為2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2
溫馨提示
- 1. 本站所有資源如無特殊說明,都需要本地電腦安裝OFFICE2007和PDF閱讀器。圖紙軟件為CAD,CAXA,PROE,UG,SolidWorks等.壓縮文件請下載最新的WinRAR軟件解壓。
- 2. 本站的文檔不包含任何第三方提供的附件圖紙等,如果需要附件,請聯系上傳者。文件的所有權益歸上傳用戶所有。
- 3. 本站RAR壓縮包中若帶圖紙,網頁內容里面會有圖紙預覽,若沒有圖紙預覽就沒有圖紙。
- 4. 未經權益所有人同意不得將文件中的內容挪作商業或盈利用途。
- 5. 人人文庫網僅提供信息存儲空間,僅對用戶上傳內容的表現方式做保護處理,對用戶上傳分享的文檔內容本身不做任何修改或編輯,并不能對任何下載內容負責。
- 6. 下載文件中如有侵權或不適當內容,請與我們聯系,我們立即糾正。
- 7. 本站不保證下載資源的準確性、安全性和完整性, 同時也不承擔用戶因使用這些下載資源對自己和他人造成任何形式的傷害或損失。
最新文檔
- T/LTXH 002-2023“天賦河套”區域公用品牌黃柿子汁
- T/TMAC 094-2024公路工程玄武巖纖維復合筋設計與施工規范
- 江蘇省蔬菜買賣合同4篇
- 上海二建試題及答案
- 2025年舞蹈教練聘用合同2篇
- 個體經營短期借款協議書8篇
- 晚會演出合同協議書范本3篇
- 文娛與體育課件
- 2025遼寧師范大學輔導員考試試題及答案
- 2025益陽教育學院輔導員考試試題及答案
- 人保農險理賠試題
- Machine-Cmk-設備能力指數Cmk分析表
- 心理健康教育特色學校建設路徑
- 2025年全國保密教育線上培訓考試試題庫【完整版】附帶答案詳解
- (二模)2025年5月濟南市高三高考針對性訓練英語試卷(含答案解析)
- 修腳師勞動合同(新標準版)6篇
- TCHSA-012-2023-兒童口腔疾病治療中靜脈鎮靜技術規范
- ISO27001:2022信息安全管理體系全套文件+表單
- 大學體育與體質健康(山東聯盟)智慧樹知到期末考試答案章節答案2024年中國石油大學(華東)
- 網絡食品交易第三方平臺備案表
- Dell 2950 SAS5RAID完全配置手冊

評論
0/150
提交評論