



版權說明:本文檔由用戶提供并上傳,收益歸屬內容提供方,若內容存在侵權,請進行舉報或認領
文檔簡介
1、人呼吸道合胞病毒Long株的免疫原性初探李華楊婷岳盤劉正玲姜廣菊龍洞鄉楊蓉羅芳宇謝忠平摘要目的評價人呼吸道合胞病毒(HRSV)Long株的免疫原性,為進一步的研究疫苗提供實驗數據。方法將HRSV制備成純化抗原,取40只ICR鼠.隨機分為4組,分別用純化HRSV、純化HRSV+Al(OH),、并設0.01mol/LPBS、A1(OH),對照組,0天、28天免疫小鼠,采用中和試驗檢測血清中和抗體,流式檢測7種細胞因子。結果初免后28天,加AKOH),組與無AKOH),組抗體陽轉率分別為60%和50%,抗體幾何平均效價(GMT)分別為1:4.49和1:5.27;加強免疫后,A1(OH),組與無A1(
2、OH)3組小血清抗體陽轉率均達100%,抗體幾何平均效價(GMT)分別為I:17.15和1:10.56,平均增長3.8倍和2.0倍;中和抗體在組間無差異,而組內初免與再免的中和抗體有統計學差異(P<0.01)6加A1(OHL樣品組與無Al(OH),樣品組,所檢測7種細胞因子均誘導IL-6及TNF,與兩個對照組間有統計學差異(P<0.05),而另外5種細胞因子則無明顯升高。結論人呼吸道合胞病毒Long株可產生良好的免疫效應。關鎧詞人呼吸道合胞病毒Long株細胞因了免疫原性中圖分類號R373.1文獻標識褐AEvaluationoftheImmunogenicityofHumanResp
3、iratorySyncytialVirusLongStraininMice.LiHua,YangTing,YueLei,etal.InstituteofMedicalBiology,PekingUnionMedicalCollege,ChineseAcademyofMedicalScience,YunnanProvincialEngineeringandTechnologicalResearchCenltrJorDevelopmentofVaccinesagainstMajorInfectiousDiseases,YunnanProvincialKeylaboratoryforDevelopm
4、entofVaccinesagainstMajorInfectionsDisease,Yunnan650118ChinaAbstractObjectiveToevaluateimmunogenicityofhumanrespiratorysyncytialvirus(HRSV)Longstrainandprovideexperimentaldataforfurtherresearch.MethodsHKSVwaspreparedaspurifiedantigenbycellculture,columnchromatography.Then,forty4-weekoldICRmiceweredi
5、videdintofourgroupsandinoculatedtwicewithHRSV,HRSV+Al(OH),PBS,andAl(OH),respectivelyat0and28days.Theserumneutralizingantibodyliterwasanalyzedbymicro-neutralizationtestinvitroandvariouscytokinesweredeterminedbyflowcytometry.ResultsSeroconversionratesofHRSV+Al(OH),groupandHRSVgroupwere60%and50%at28day
6、safterthefirstinoculation,andantibodygeometricmeantiters(GMT)were1:4.49and1:5.27.SeroconversionratesofHRSV+Al(OH),groupandHRSVgroupwere100%at7daysafterthesecondinoculation,andantibodygeometricmeantiters(GMT)were1:17.15(3.8-fold)and1:)0.56(2-fold).NeutralizingantibodiesbetweenHRSV+Al(OH),groupandHRSV
7、grouphadnodifferences,whileneutralizingantibodiesbetweentheinoculationshadsignificantlydifferences(P<0.01).IL-6andTNFofHRSV+A)(OH)jgroupandHRSVgroupbothincreasedsignificantlycomparedwithcontrolgroup(P<0.05).ConclusionHumanrespiratorysyncytialvirus(HRSV)Longstraincaninduceimmuneresponseeffectiv
8、ely.KeywordsHumanrespiratorysyncytialvirus(HRSV);Longstrain;Cytokine;Immunogenicity人類呼吸道合胞病毒(humanrespiratoryvirus,HRSV)是世界范圍內嬰幼兒病毒性下呼吸道感染最重要的病原體,尤見于嬰幼兒、老年人及免疫缺陷病人等急性呼吸道感染住院者m。據估計,每年在世界范圍內有3400萬6500萬的呼吸道合胞病毒感基金項目:國家高技術研究發展計劃(863)基金資助項目(2012AA02A404);云南省應用基礎研究面上項目(2011FZ2I0)作者單位:650118昆明,中國醫學科學院/北京協和
9、醫學院醫學生物學研究所云南省敢大傳染病疫苗工程技術研究中心,云南省重大傳染病疫苗研發放點實驗室通訊作者:謝忠平,電子信箱:xzp218染病例和16.0萬19.9萬死亡病例,僅在美國,呼吸道合胞病毒導致每年住院大約12.5萬例。在發展中國家,RSV在嬰幼兒引起急性下呼吸道感染的病死率比較高。由于該病毒的高感染率,在1歲前近70%的兒童就被首次感染,更重要的是,2歲以下嬰兒大約36%至少感染兩次0引。從1956年Mor-ris等首次發現該病毒至今,RSV感染引起的社會經濟負擔實際上比季節性流感更加嚴重,給國家和個人帶來極大的損失。雖然HRSV疫苗的研究已有50多年的歷史,但至今尚無被批準使用的產品
10、。因此,WHO已將呼吸道合胞病毒疫苗列為21世紀需要優先解決的問題之-0由于IIRSV自然感染激發的機體免疫是不完全免疫,需再次或多次的HRSV感染才能完善,疫苗需要多次給荷才能達到保護嚴幣下呼吸道感染的免疫水平。因此.獲得免疫原性高的病毒株,才能為后續制備RSV單克隆抗體及裂解疫苗的研究打下基礎”鑒FRSV感染后,T細胞亞群、細胞因子在致病和抗病中有著幣:要的作用。對Thl/Th2細胞因子的研究,在RSV疫苗及治療藥物方而有樣枳極意義。至今對KSV的研究已經涉及很多方面,但對RSVA亞型山嘩株免疫原性的基礎研究還未見報道,現將結果報道如下。材料與方法1. 材料:(1)細胞和病毒:Hep-2細
11、胞、KMB”細胞由本所質質檢定室提供;RSV修叫株購于中國典型培養物保藏中心。(2)主要儀器和試劑:BDFACSCanto【I流式細胞儀為I巾公司產品;IW聯免疫分析儀/多功能生物檢測儀為美國BIOTEK公司產品;Bl()-RAI)Chemi!)<><rMImagingSystem為美國BIO-RAD公司產品;一抗:兔抗RSVIgC為美國IMG-ENEX公司產品;半抗兔-HRP為alxarn公司產品;AI(0H),佐劑(濃度為2.0mg/ml)為本所甲肝疫苗生產室自制;BDCytomrlricBead.Xrray(CBA)MouseThl/Th2/Thl7CytokineKi
12、t(lol:3072948),購于BD公司;化學發光底物:ImmobilonWesternChemiluminecentHRPSubstrate(lot:1131801),購于Milliport*公司。(3)實驗動物:清潔級ICR(InstituteofCancerResearch)小鼠,4周齡,雌旋各半,體9(16-18g,由筆者單位靈長類中心小動物部提供實臉動物合格證弓:SYXK(滇)2010007,2. 方法:(1)實撿性疫苗制務:取生K狀態良好的致密單ISHep2細胞,培養并收狀病誰;初純、超濾濃縮;選擇Seph-arosIFF凝膠”純化.用雙抗體夾心法檢測RSV抗原含時.將RSV抗原
13、含W而的不同收集樣品合并即為純化的HRSV樣品,合并的樣品用30kDa的超濾離心管.4000r/min,20min離心濃縮純化HKSV加AI()H),或不加AI(OH),制備成為實輪組樣品(2)純化產物的檢測:不同純化收集的產物經SDS-PAGE電泳;濃筋后樣品用蛋白檢測試劑盒PierceBCAProleinAssayKit檢測蛋白含仙,具體方法見試劑盒說明B;Westernblot法鑒定SDS-PAGE電泳,半干轉印至PDVF股上.以5%脫脂奶粉37Y封閉lh后,加-抗(兔抗RSVIgG多克隆抗體,濃度I:500)4T過夜、加二抗(乍抗兔IgG-HRPI:500)37T反應lh,化學發光底物
14、曝光顯影>(3)免疫原性評價:選取ICK小鼠40只.隨機分為4組,每組10只。2組實輪性樣品:純化HRSV組無AI(OH),佐劑、純化HRSV+Ai(OH)j佐削組AI(0H使用濃度為l.0mg/ml;同時設兩個對照m:0.01mol/LPBS(pH7.4)對照組、AI(OH),對照組O.OImol/LPBS(pH7.4)配制的l.0mg/mlA1(OH)3佐劑。免疫注射劑景:每只0.5ml,腹腔注射。免疫程序:分別于0天、28天免疫.共免疫2次.于初免后28天、加強后7天采血分離血清,檢測血清中和抗體效價及IL-2JL-4JL-6JFN-7JNFJL-17AJL-IO共7種細胞因于“(
15、4)血清中和抗體效價檢測:采用固定羯荏稀釋血清的微砒中和試驗法來檢測血清中和抗體效價。待測血清56弋滅活30min后,做2倍系列稀釋.每稀料度50微升/孔,可加入2000CCID/ml病毒50微升/孔,混勻,37*中和lh后,加入IxIO6/ml濃度的Hep-2細胞100微升/孔.置37Y、4%CO,孵箱中培葬。同時設置病毒對照、細胞對照和明性血清對照。于第7天判定結果。以抗體效價Nl:4為陽性。(5)血清細胞因子的檢測:用BD公BDCytometricBeadArray(CBA)Moum*Thl/Th2/Thl7CytokineKit,流式細胞儀檢測小鼠血清中的IL-2等7種細胞因子。具體方
16、法見試劑食說明書°3.統計學方法:使用SPSS13.0軟件進行數據的統計分析分別對組間進行比較.對于不滿足正態分布的,采用非參數檢臉的方法進行比較;滿足正態分布旦方差齊性,采用兩獨立樣本的,檢驗.以P<0.05為差異行統計學意義。結果1. Sepharose4FF凝膠過濾層析法純化樣品:收獲病毒液感染性效價為6.l25lgCCID“/ml,抗原效價為1:64,純化得率為44.4%。Sepharose4FF凝膠過濾純化曲線(圖I)。圖1Sepharose4FF凝膠過浦層析法純化樣品的純化曲線2. SDS-PAGE電泳和Westernblot:經檢測RSV抗原含量高的樣品合并,用5
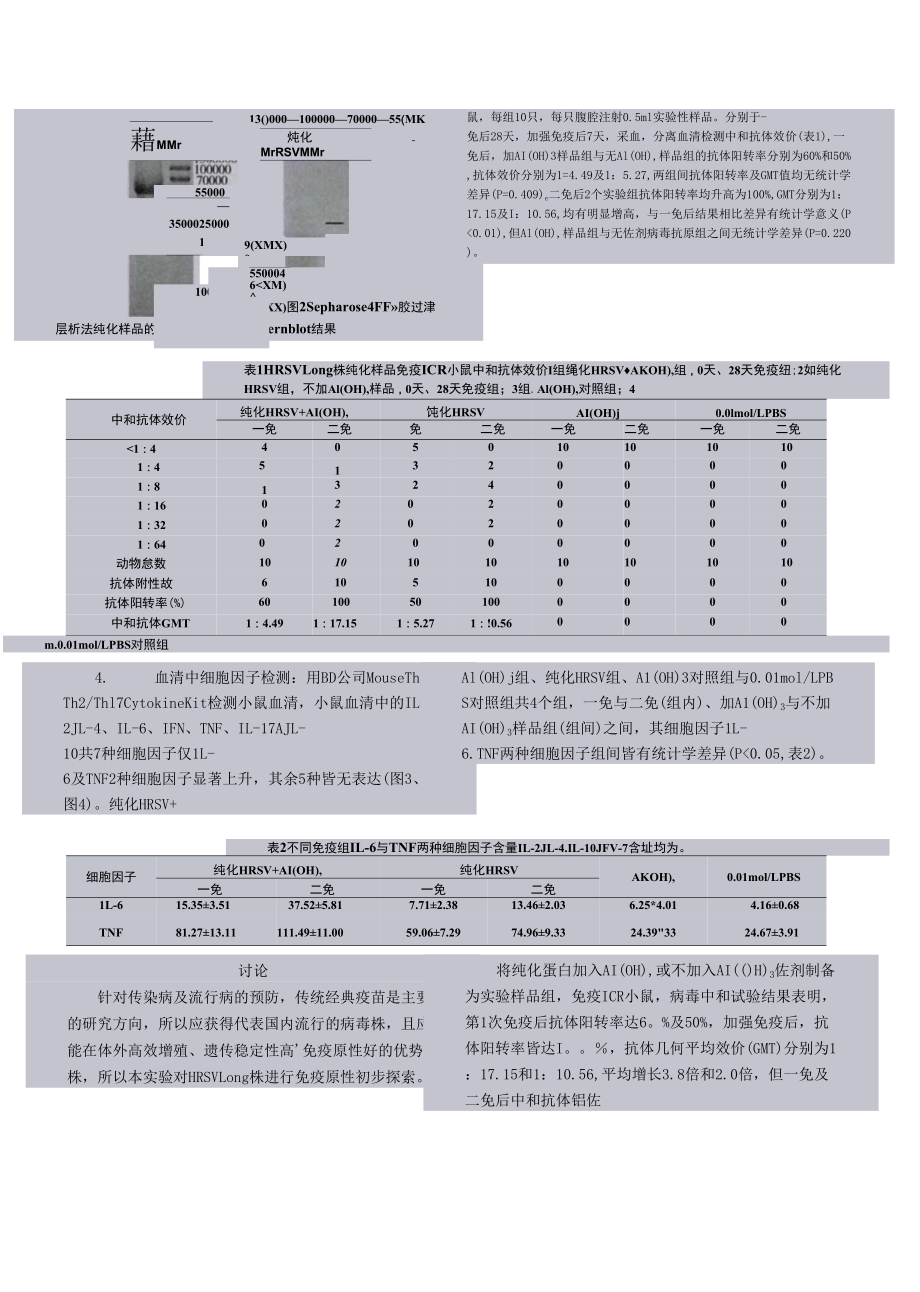
17、0kl)a的離心管離心濃縮,即為實驗樣品,SDS-PAGE電泳,Bio-Rad的QuantityOne軟件分析表明,純度達95%以上。Westernblot檢測,可見為3個條帶:G蛋白90kDa、F蛋白55k【)a及N蛋白46kDa(圖2)。用蛋白檢測試劑盒檢測蛋白含址為3.66mg/mlo3. HRSV純化樣品的中和抗體:將樣品合并濃縮后,加AI(OH),或不加AI(OH)3制備成實驗性樣品。經免疫程序(一免1針或二免2針)免疫ICR小550005500010000350002500015000藉MMr9(XMX)05500046<XM)燉化MrRSVMMr13()0001000007
18、000055(MK)35()002S(XX)圖2Sepharose4FF»膠過津層析法純化樣品的SDS-PAGE和Westernblot結果鼠,每組10只,每只腹腔注射0.5ml實驗性樣品。分別于-免后28天,加強免疫后7天,采血,分離血清檢測中和抗體效價(表1),一免后,加AI(OH)3樣品組與無Al(OH),樣品組的抗體陽轉率分別為60%和50%,抗體效價分別為1=4.49及1:5.27,兩組間抗體陽轉率及GMT值均無統計學差異(P=0.409)e二免后2個實驗組抗體陽轉率均升高為100%,GMT分別為1:17.15及I:10.56,均有明顯增高,與一免后結果相比差異有統計學意義
19、(P<0.01),但Al(OH),樣品組與無佐劑病毒抗原組之間無統計學差異(P=0.220)。表1HRSVLong株純化樣品免疫ICR小鼠中和抗體效價I組繩化HRSVAKOH),組,0天、28天免疫紐;2如純化HRSV組,不加Al(OH),樣品,0天、28天免疫組;3組.Al(OH),對照組;4中和抗體效價純化HRSV+AI(OH),飩化HRSVAI(OH)j0.0lmol/LPBS一免二免免二免一免二免一免二免<1:44050101010101:4513200001:8132400001:16020200001:32020200001:6402000000動物怠數10101010
20、10101010抗體附性故6105100000抗體陽轉率(%)60100501000000中和抗體GMT1:4.491:17.151:5.271:!0.560000m.0.01mol/LPBS對照組4. 血清中細胞因子檢測:用BD公司MouseThl/Th2/Thl7CytokineKit檢測小鼠血清,小鼠血清中的IL-2JL-4、IL-6、IFN、TNF、IL-17AJL-10共7種細胞因子僅1L-6及TNF2種細胞因子顯著上升,其余5種皆無表達(圖3、圖4)。純化HRSV+Al(OH)j組、純化HRSV組、A1(OH)3對照組與0.01mol/LPBS對照組共4個組,一免與二免(組內)、加
21、A1(OH)3與不加AI(OH)3樣品組(組間)之間,其細胞因子1L-6.TNF兩種細胞因子組間皆有統計學差異(P<0.05,表2)。表2不同免疫組IL-6與TNF兩種細胞因子含量IL-2JL-4.IL-10JFV-7含址均為。細胞因子純化HRSV+AI(OH),純化HRSVAKOH),0.01mol/LPBS一免二免一免二免1L-615.35±3.5137.52±5.817.71±2.3813.46±2.036.25*4.014.16±0.68TNF81.27±13.11111.49±11.0059.06±
22、7.2974.96±9.3324.39"3324.67±3.91討論針對傳染病及流行病的預防,傳統經典疫苗是主要的研究方向,所以應獲得代表國內流行的病毒株,且應能在體外高效增殖、遺傳穩定性高'免疫原性好的優勢毒株,所以本實驗對HRSVLong株進行免疫原性初步探索。將純化蛋白加入AI(OH),或不加入AI()H)3佐劑制備為實驗樣品組,免疫ICR小鼠,病毒中和試驗結果表明,第1次免疫后抗體陽轉率達6。%及50%,加強免疫后,抗體陽轉率皆達I。,抗體幾何平均效價(GMT)分別為1:17.15和1:10.56,平均增長3.8倍和2.0倍,但一免及二免后中和抗體
23、鋁佐圖3純化HRSVLong株免疫小版不同組別IL-6含A.純化HRSVAKOH),組第次免疫小M.;B.純化HRSV+AI(OH)j蛆第2次免疫小鼠;C.純化ilRSV第1次免疫小鼠:D.純化HRSV組第2次免疫小鼠;E.Al(OH):對照組;F.0.01mol/LPBP對照組50454035302520151050wox)olow)o。4<2O<86<4I2111(wl)IS:&XNf-a-左昌圖4純化RSVLong株免疫小鼠不同組別TNF含A.純化HRSV+AKOH),組第I次免疫小鼠;B.純化HRSV»Al(OH)j祖第2次免疫小鼠;C.純化IIRS
24、V祖第I次免疫小隊;D.純化HKSV組第2次免疫小鼠;E.AI(OH)j對照祖;F.0.Olmol/LPBP對照組劑組與無佐劑組GMT差異皆無統計學意義。抗體水平顯著升高,但是效價較低,這與文獻7報道的RSVA2株的免疫結果相符。實驗雖然不是同一病毒株,但都屬于A亞型,究其原因:是否由于RSV病毒是有包膜的病毒,經過病毒的初純、超濾濃縮、凝膠純化及再濃縮(超濾離心)一系列處理對病毒的影響所導致。另一個原因是否由于該毒株的生物學特性及基因編碼與其他病毒的具體差異所致,在獲得RSVLong株后,對病毒株擴大培養至第5代,并進行RT-PCR擴增病毒的F基因、G基因及N基因,將測序結果進行比對(比對株
25、GenBank登錄號:AY911262.1):RSV-N蛋白核昔酸同源性為97.48%,RSV-F蛋白為94.01%,RSV-G蛋白為99.78%。該毒株的F蛋白同源性較G蛋白低,與文獻報道不一致,但都大于90.00%,同源性的差異是否與血清效價有直接關系,有待進步實驗。20世紀60年代研制的甲醛滅活疫苗(F1-RSV)的研究發現,HRSV滅活疫苗具有疾病加強作用,可能原因是破壞了小鼠輔助性T細胞Thl和Th2亞群動態平衡狀態。本次研究小鼠血清的細胞因于實驗結果顯示,僅有1L-6及TNF2種細胞因子升高,而IFN-7JL-4JL-2皆未升高。實驗中A1(OH、佐劑的使用,主要于注射位點的沉積.
26、誘導動物模型的Th2型免疫應答,但結果顯示佐劑的使用并未顯著增加HRSV的免疫效果,所產生的抗體與無佐劑組無顯著差異"°)。所以該RSVLong株所誘導的免疫是平衡的,未見明顯的疾病加強指標。另外,IL-6及TNF2種細胞因子的升高,是否可以從以下得到解釋:Levitz等山報道無論是在體內和體外,IL-6促炎細胞因子是宿主對呼吸道合胞病毒感染的反應產物。Pribul等發現肺部早期趨化因子分泌的峰值是由巨噬細胞驅動,肺泡巨噬細胞受激活導致大量促炎癥細胞因子的產生包括MIPla、TNF-a、IL-6、IL-8。實驗所檢測的IL-6及TNF2種細胞因子升高,是否由于肺泡巨噬細胞激
27、活所致尚待進一步證實cChoi等”報道腫瘤壞死因子(TNF)與兒童呼吸道感染RSV引起嗜酸性粒細胞炎癥有關。研究還發現,人外周血多形核顆粒細胞(PMN)感染RSV后可分泌IL-6JIIL-6的含量與接觸病毒的數所有密切關系,Grell等報道的IL-6的產生呈現年齡依賴性,即年齡越小的動物越容易產生。綜上所述,如何在保持免疫原性的基礎上,使RSV病毒樣品能誘導平衡的Thl/Th2反應,增加疫苗的安全性,是RSV疫苗研究的關鍵。本實驗初步探討了RSVLong株抗原的免疫原性,從實驗結果分析,本研究所制備的HRSV能誘導產生明顯的體液免疫及細胞免疫,為進一步系統研究HRSV疫苗提供了實驗資料。參考文
28、獻1 RobinsonKA.OdelolaOA,SaldanhaU.etal.PalivizumabforprophylaxisagainstrespiratorysyncytialvirusinfectioninchildrenwithcysticGbrosisfJ.CochraneDatabaseSystRev,2012,2:C1X)07743SchmidtMR,McGinnesLW,KenwardSA,elal.Long-termandmemoryimmuneresponsesinmiceagainstnewcastlediseasevirus-likeparticlescontaini
29、ngrespiratorysyncytialvirusglycoproteincctodo-mainsfJ,JVirology.2012,86(21):11654-116622 StoreyS.Respiratorysyncytialvirusmarket.NaturereviewsJ.DrugDiscovery2010,9:15-16NairH.NokesDJ.GeiwnerBD.eial.Globalburdenofacutelowerrrspiratoryinfectionsduetorespiratorysyncytialvirusinyoungchildren:asystematic
30、reviewandmela-analysisJ.lancet.2010,375:1545-15553 張竟,佝浩林.梅興國.呼吸道合胞病毒(RSV)與Thl/Th2細胞因子的關系研究進展J.沈陽藥科大學學報,2008,25(12):1016-1020金奇,畢勝利,陳繼明.醫學分子病毒學M.北京:科學出版社,2001:461-4796 童莉蛆,李華,蔣乾物,等.人呼吸道合胞病毒不同純化方法的比較研究J.醫學研究雜志,2011.40(4):73-76李光,井申榮.呼吸道合胞病毒蛋白的研究進展J).中國生物制品雜志,2006,19(5):541-5477 BrewerJM.ConacherM,Sat
31、oakerA.etal.Ininterleukin-4-deficientmice,alumnotonlygeneratesThelper1responsesequivalenttoFreund'scompleteadjuvant,butcontinuestoinduceThelper2cytokineproductionJ.EURJImmunol,1996,26(9):2062-2066MosmannTR,CherwinskiH,BondMW.elal.TwotypesofmurinehelperTcellclone.I.Definitionaccordingtoprofilesof
32、lymphokineactivitiesandsecretedproteinsJ.JImmunol.1986,136(7):2348-2357LevitzR,WattierR.PhillipsP,etal.InductionofIL-6andCCL5(RANTES)inhumanrespiratoryepithelial(A549)cellsbyclinicalisolatesofrespiratorysyncytialvirusisstrainspecificJ.Virol,2012,(190)9:l-98 PribulPK,HarkerJ,WangB,etal.Alveolarmacrop
33、hagesareamajordeterminantofearlyresponsestovirallunginfectionbutdonotinfluencesubsequentdiseasedevelopmenttJ.JVirol.2008,82(9):4441-4448ChoiJ,CallawayZ,KimHB,elal.TheroleofTNF-aineosinophilicinflammationassociatedwithRSVbronchiolitisJ.PediatricAllergyImmunology,2010,21:474-479(收稿日期:2013-12-25)(修回日期:
34、2013-12-30)人結直腸癌細胞Drosha基因敲除細胞模型的構建李蕓僑李尚澤宋偉王任先張曉東王琳芳摘要目的為研究核酸酶Drosha與結直腸癌的關系,利用腺相關病毒(AAV)介導的染色體同源重組技術,構建Drosha基因敲除的HCT116結直腸癌細胞模型。方法設計引物通過PCR擴增Drosha基因的同源臂,構建Drosha的AAV病毒打靶栽體,通過病毒的包裝、感染、抗生素新霉素(G418)藥物篩選、PCR以及Westernblot鑒定獲得基因敲除陽性細胞株,通過Cre病毒感染去除抗性基因,最終建立敲除Drosha基因的結直腸癌細胞模型。結果經過兩輪打靶,分別將DNA雙輕上的Drosha基因
35、去除并經Westernblot鑒定,獲得Drosha-/-陽性的HCTU6細胞株。結論通過AAV病毒介導的染色體同源重組技術,成功構建Drosha基因敲除的HCT116細胞系。關鍵詞基因敲除Drosha同源重組結直腸癌中圖分類號R735文獻標識袒AEstablishmentofDrosha-/-cellModelinHCT116.LiYurujiao,LiShangze,SongWei,etal.StateKeyLaboratoryofMedicalMolecularBiology,InstituteofBasicMedicalSciences,CAMSandSchoolofBasicMedicine,PUMC,Beijing10000
溫馨提示
- 1. 本站所有資源如無特殊說明,都需要本地電腦安裝OFFICE2007和PDF閱讀器。圖紙軟件為CAD,CAXA,PROE,UG,SolidWorks等.壓縮文件請下載最新的WinRAR軟件解壓。
- 2. 本站的文檔不包含任何第三方提供的附件圖紙等,如果需要附件,請聯系上傳者。文件的所有權益歸上傳用戶所有。
- 3. 本站RAR壓縮包中若帶圖紙,網頁內容里面會有圖紙預覽,若沒有圖紙預覽就沒有圖紙。
- 4. 未經權益所有人同意不得將文件中的內容挪作商業或盈利用途。
- 5. 人人文庫網僅提供信息存儲空間,僅對用戶上傳內容的表現方式做保護處理,對用戶上傳分享的文檔內容本身不做任何修改或編輯,并不能對任何下載內容負責。
- 6. 下載文件中如有侵權或不適當內容,請與我們聯系,我們立即糾正。
- 7. 本站不保證下載資源的準確性、安全性和完整性, 同時也不承擔用戶因使用這些下載資源對自己和他人造成任何形式的傷害或損失。

評論
0/150
提交評論